发布时间:2021-09-27所属分类:工程师职称论文浏览:1次
摘 要: 摘要:目的建立HPLC法测定盐酸氨溴索口服液中蔗糖和山梨醇含量的方法,并考察全国范围内20个生产企业的添加情况。方法采用HYPERSIL氨基色谱柱(4.6mm250mm,5m),以乙腈-水(80﹕20,V/V)为流动相,流速1.0mLmin-1,柱温为35℃,示差折光检测器。结果盐酸氨溴
摘要:目的建立HPLC法测定盐酸氨溴索口服液中蔗糖和山梨醇含量的方法,并考察全国范围内20个生产企业的添加情况。方法采用HYPERSIL氨基色谱柱(4.6mm×250mm,5μm),以乙腈-水(80﹕20,V/V)为流动相,流速1.0mL·min-1,柱温为35℃,示差折光检测器。结果盐酸氨溴索与蔗糖和山梨醇均能良好分离,并分别在1~10mg·mL-1范围内,蔗糖(r=0.9996,n=6)、山梨醇(r=0.9999,n=6)线性关系良好;定量限分别为8.03和8.04μg;平均回收率(n=9)分别为101.0%和100.9%,RSD分别为1.03%和0.97%。对全国范围内20个生产企业的样品进行测定,个别企业测定的结果与生产处方不一致。结论所建方法简单易行,准确可靠、重复性良好,为测定口服溶液中矫味剂的添加情况及质量评价奠定了基础。
关键词:盐酸氨溴索口服液;蔗糖;山梨醇;高效液相色谱;示差折光
口服溶液经常会添加矫味剂,以掩盖药物的咸、涩和苦味,包括天然和人工合成二大类,大部分甜味剂是人工合成的,大量摄入会产生一定的毒副作用,会导致高血糖、肥胖等代谢性疾病,可能还有一定的致癌性[1-2],且儿童为口服溶液的主要使用群体,所以甜味剂在使用过程中必须严格控制用量[3]。
此次国评共收集到22个生产企业的盐酸氨溴索口服液,根据生产厂家提供的生产工艺和资料分析,口服溶液中使用甜味剂主要阿司帕坦、AK糖、糖精钠、山梨醇、蔗糖等。查阅文献,已有报道大多采用紫外检测的方法,但对于没有紫外吸收的蔗糖、山梨醇等未能检测[4-10],而此两种矫味剂应用最多。本文建立了高效液相色谱-示差折光检测的方法测定蔗糖、山梨醇的添加量,同时考察了全国范围内该产品的添加情况。阿司帕坦、AK糖、糖精钠和本产品的抑菌剂采用高效液相色谱-紫外检测器检测(另有研究报告)。
1仪器与试剂
1.1仪器Agilent1260高效液相色谱仪(配备DAD检测器),瑞士梅特勒电子分析天平(型号:XPE205),高纯水机(美国Millipore公司)。
1.2试药及试剂
试药:22个生产企业的63批样品均来自2020年国家评价性抽验样品。山梨醇(批号:F675G,企业提供);蔗糖(批号:FL1001200311-1,企业提供)。试剂:乙腈(Sigma,色谱纯),超纯水。
2方法与结果
2.1色谱条件
采用HYPERSIL氨基柱(4.6mm×250mm,5μm);流动相:乙腈-水(80﹕20,V/V);示差折光检测器;柱温:35℃;流速:1.0mL·min-1;进样体积:20µL。
2.2溶液的制备
2.2.1系统适用性溶液分别取山梨醇、蔗糖原料各适量,加水溶解并稀释制成5mg·mL-1的溶液,作为系统适用性溶液。系统适应性色谱图见图1。理论板数分别按山梨醇和蔗糖计算,应大于2000,山梨醇与蔗糖的分离度应不小于1.5。
2.2.2标准曲线的制备分别取山梨醇、蔗糖原料各适量,加水溶解并稀释制成10mg·mL-1的溶液作为对照品贮备溶液。将对照品贮备溶液逐级稀释成浓度分别为1,3,4,6,10mg·mL-1的线性对照溶液。
2.2.3供试品溶液的制备根据山梨醇、蔗糖的处方量,精密量取盐酸氨溴索口服溶液适量,加水溶解并稀释制成各含山梨醇、蔗糖分别为3~6mg·mL-1的溶液,摇匀,作为供试品溶液。
2.3方法学验证
2.3.1线性关系依据各生产企业处方涉及甜味剂的线性范围,4种防腐剂和山梨醇及蔗糖标准曲线溶液配置方法参照“2.2.2”项。以对应的色谱图峰面积为纵坐标(y),质量浓度为横坐标(x,mg·mL-1)进行回归分析。线性方程分别为:山梨醇y=2.15×105x-7.45×104,r=0.9996;蔗糖y=2.15×105x-1.51×105,r=0.9999。结果表明,山梨醇、蔗糖在各自浓度范围内线性关系良好。
相关知识推荐:比较容易发表药学类论文的省级以上期刊??
2.3.2重复性试验企业18的生产处方既添加了蔗糖又添加了山梨醇,故选择企业18的某一批样品(批号:200107)按照“2.2.3”项下平行制备6份溶液,进行重复性考察,6份样品中山梨醇、蔗糖测得含量的RSD均分别为0.62%和1.44%,均小于2.0%。
2.3.3精密度试验将对照溶液(6mg·mL-1)重复进样6次,山梨醇、蔗糖峰面积的RSD分别为1.75%和1.70%,均小于2.0%。
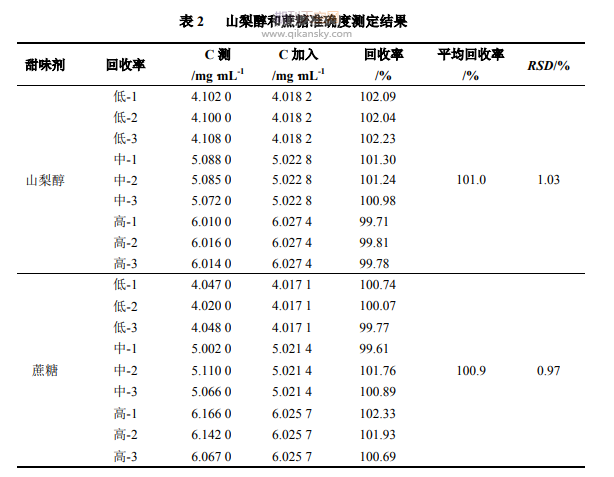
2.3.4准确度试验将除过山梨醇、蔗糖外,处方中的其他组分按照处方量混匀作为空白基质,再将山梨醇、蔗糖对照贮备液按照处方80%,100%,120%加入,每个浓度平行制备3份样品,共9份样品。按照供试品制备方法同法处理,即得。测定结果见表2。
由于山梨醇在处方中的含量在5%~30%之间,蔗糖在处方中的含量在0.1%~30%之间,根据2020年版中国药典四部9101规定[11],山梨醇、蔗糖的平均回收率分别为101.1%、100.9%,RSD分别为1.03%、0.97%,均符合规定,表明所建立的方测定2种甜味剂含量准确度良好。
2.3.5检测限和定量限以线性1mg·mL-1溶液逐步稀释,以S/N=3的浓度为检测限,以S/N=10的浓度为定量限,结果见表3。
2.3.6专属性试验取空白溶液、流动相、除山梨醇蔗糖外的辅料混合溶液和盐酸氨溴索溶液进样,在山梨醇和蔗糖色谱峰位置处均未出峰,证明无干扰,色谱图见图2。
2.4样品测定采用所建立的方法对20家生产厂家50批样品进行测定,采用外标法定量,结果见表4。样品相关图谱见图3。
各生产企业样品山梨醇与蔗糖的测得量,与其生产处方比较,由上表可知:山梨醇的测定结果占处方加入比为94%~107%,与处方基本一致;而蔗糖的测定结果占处方加入比为19%~100%,部分企业测定结果较加入量偏低,与处方规定量有较大出入。
3讨论
3.1色谱柱的选择
实验开始选用资生堂CAPCELLPAKC18MGⅡ(4.6mm×250mm,5μm)色谱柱,采用乙腈-水体系,改变比例,山梨醇及蔗糖均未出峰。更换为ThermcAPS-2HYPERSIL氨基柱(4.6mm×250mm,5μm),采用流动相比例乙腈-水体系,检出山梨醇和蔗糖,且能良好分离度。
3.2流动相的选择
选用甲醇-缓冲盐体系,色谱峰形较差,无法分开待测成分。更换我乙腈-水体系,峰形得到很大改善,乙腈比例越大,分离度变好,最终选取乙腈-水(80﹕20,V/V)作为流动相。
3.3测定结果分析
本次实验所测得蔗糖量占处方加入比为19%~100%,部分企业测定结果较加入量偏低较多,与处方规定量有较大出入。分析原因:一是矫味剂加入不足;而是在生产过程中有损失。矫味剂关系不仅关系到产品的口感,更关系到内在质量,比如酸碱度、微生物指标等。建议企业分析原因,严格规范矫味剂使用。——论文作者:王小亮,席志芳,张秉华,梁亚伟,邓玉龙
SCISSCIAHCI