0
发表咨询在线!

发布时间:2021-09-28所属分类:医学职称论文浏览:1313次
摘 要: 摘要目的:建立肤康凝胶的质量标准。方法:采用高效液相色谱法测定制剂中苦参碱、黄芩苷的含量。结果:苦参碱浓度线性范围为18.56~296.96g/ml(R=0.9996),黄芩苷浓度线性范围为8.325~416.262g/ml(R=1),精密度、稳定性、重复性试验RSD均小于3.0%,加样回收

摘要目的:建立肤康凝胶的质量标准。方法:采用高效液相色谱法测定制剂中苦参碱、黄芩苷的含量。结果:苦参碱浓度线性范围为18.56~296.96μg/ml(R²=0.9996),黄芩苷浓度线性范围为8.325~416.262μg/ml(R²=1),精密度、稳定性、重复性试验RSD均小于3.0%,加样回收率分别为97.09%~99.63%(RSD=1.016%,n=6),92.04%~94.43%(RSD=1.111%,n=6)。结论:所建立的研究方法稳定、可靠、重复性好,可用于肤康凝胶的质量控制。
关键词肤康凝胶苦参碱黄芩苷高效液相色谱法
肤康凝胶是院内制剂复方苦参洗剂通过剂型优化而成,该处方由我院皮肤科省级名中医根据多年临床经验,在中医古方“苦参汤”的基础上研制而成,具有清热解毒、燥湿止痒之功效,并经过长期临床应用,在治疗湿疹、皮肤脓疱疹及红痱等瘙痒性、感染性皮肤病方面疗效显著,深受患者的欢迎,已成为皮肤科中医治疗的优势药物[1]。临床上由于中药洗剂存在用量大、携带使用不方便、病人依从性差等因素,故将其改造成具有生物相容性好,制备工艺简单,局部给药后易吸收、易清洗、使用舒适的外用凝胶,克服原剂型的缺陷,更好地发挥其显著疗效,提升我院新制剂的研制水平。为保证该制剂质量的稳定可控,安全有效,本文采用高效液相色谱法(HPLC)测定苦参碱及黄芩苷的含量,以建立肤康凝胶的质量标准。
1仪器与材料
1.1仪器与设备:高效液相色谱仪(日本岛津LC-20AT型,SPD-20A型紫外可见检测器);RE-200B旋转蒸发仪(上海亚荣生化仪器厂);DHG9246A电热恒温鼓风干燥箱(上海精宏实验设备有限公司);DK-S24电热恒温水浴锅(上海精宏实验设备有限公司);XS105DU分析天平(梅特勒-托利多仪器有限公司d=0.01mg);BT224S电子分析天平(赛多利斯科学仪器有限公司d=0.1mg);BY-G16型高速医用离心机(北京白洋医疗器械有限公司);OKO-PN电动喷雾器(武汉药科新技术开发有限公司);YOKO-PX薄层显色抽气箱(武汉药科新技术开发有限公司);ZF1-Ⅱ紫外分析仪(上海嘉鹏科技有限公司);硅胶G薄层板(青岛海洋化工厂)。
1.2药品与试剂:苦参(产地:浙江)、黄芩(产地:山西)、黄连(产地:四川)均购于浙江中医药大学中药饮片厂;苦参碱对照品(批号:110805-200508,含量100%);黄芩苷对照品(批号:110715-201619,含量93.5%)均购自中国药品食品检定研究院;肤康凝胶(批号:180520,180521,180522),阴性样品均由本实验室自制;乙醇、无水乙醇、甲醇、磷酸、乙酸乙酯、二氯甲烷、三氯甲烷均为分析纯;甲醇色谱纯、乙腈色谱纯(天津四友精细化学品有限公司)。
2方法与结果
2.1苦参碱的含量测定:分述如下。
2.1.1色谱条件[2-3]:色谱柱AgilentZORBAXNH2(4.6mm×150mm,5μm),流动相乙腈-无水乙醇-3%磷酸溶液(82∶10∶8),流速1.0ml/min;柱温30℃,检测波长220nm,进样量为10μl。理论塔板数按苦参碱峰计算应不低于2000,分离度>1.5,各成分基线分离良好。
2.1.2线性范围考察:精密称取苦参碱对照品9.28mg至25ml的容量瓶中,加乙腈-无水乙醇(80∶20)混合溶液溶解并定容至25ml,制成对照品溶液母液。分别精密吸取0.5、1、2、4、8ml置10ml容量瓶中,加乙腈-无水乙醇(80∶20)稀释至刻度,得一系列对照品溶液,浓度分别为18.56、37.12、74.24、148.48、296.96μg/ml,分别进样10μl,峰面积分别为98800、213446、434292、848252、1770232。以进样浓度x(μg/ml)为横坐标、峰面积y为纵坐标绘制标准曲线,计算得回归方程为y=5977.9x-14889(R²=0.9996),表明苦参碱在18.56~296.96μg/ml范围内线性关系良好。
2.1.3供试品溶液的制备:取本品1g至10ml量瓶中,加1ml氨水,加入适量三氯甲烷,超声30min,放置过夜,过滤,滤液蒸干,残渣加无水乙醇定容至10ml,摇匀,用0.45μm微孔滤膜滤过,取续滤液即得。
2.1.4阴性溶液的制备:按肤康凝胶处方和制备工艺制备缺苦参的阴性凝胶,按“2.1.3”项下方法制成阴性对照溶液。
2.1.5系统适应性试验:取“2.1.2”“2.1.3”“2.1.4”项下对照品溶液、供试品溶液及阴性对照溶液,按“2.2.1”色谱条件注入高效液相色谱仪测定,记录色谱图,理论塔板数按苦参碱峰计算应不低于2000,分离度>1.5,各成分基线分离良好。苦参碱对照品溶液在12.5min左右有峰,供试品在相应时间均有峰与之对应,而阴性对照溶液在12.5min左右无峰,表明其他成分对苦参碱的测定无干扰。结果见图1。
2.1.6精密度考察:精密吸取“2.1.2”项下对照品溶液,在“2.1.1”色谱条件下,连续进样6次,每次10μl,测定苦参碱的峰面积,结果,苦参碱峰面积的RSD=0.827%(n=6)。表明仪器精密度良好。
2.1.7稳定性试验:取“2.1.3”项下供试品溶液,在“2.1.1”色谱条件下于0、2、4、8、12h分别进样,进样量为10μl,测定苦参碱的峰面积,结果苦参碱峰面积的RSD=1.081%(n=6)。表明供试品溶液在12h内基本稳定。
2.1.8重复性试验:取同一批次样品6份,按“2.1.3”项下方法制备供试品溶液,按“2.1.1”色谱条件测定峰面积,记录峰面积并计算含量。结果苦参碱的RSD=1.193%(n=6)。表明本方法重复性良好。
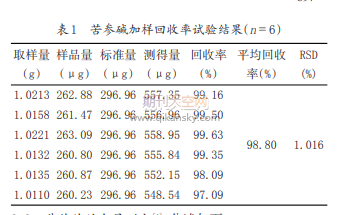
2.1.9加样回收率试验:精密称取6份已知含量的凝胶1g,分别精密加入“2.1.2”项下苦参碱296.96μg/ml对照品溶液1ml,按“2.1.3”制备。在“2.1.1”色谱条件下测定其峰面积。加样回收率(%)=[(测得量-样品量)/标准量]×100%。测得平均回收率98.80%,RSD值为1.016%。说明本方法回收率较好。结果见表1。
2.1.10样品含量测定:取3批样品各适量,分别按“2.1.3”项下方法制备供试品溶液,再按“2.1.1”项下色谱条件进样测定并计算含量,结果三批样品中苦参碱含量分别为255.712μg/g、259.086μg/g、258.106μg/g。
相关知识推荐:中医专业国家级杂志有哪些
2.2黄芩苷的含量测定[4]:分述如下。
2.2.1色谱条件:色谱柱AgilentEclipsePlusC18(4.6mm×250mm,5μm),流动相乙腈-0.1%磷酸溶液(23∶77),流速1.0ml/min;柱温30℃,检测波长280nm,进样量为10μl。
2.2.2线性范围考察:精密称取黄芩苷对照品11.13mg,加甲醇溶解并定容至25ml,制成对照品溶液母液。分别精密吸取0.5、1、2、4、8ml置25ml容量瓶中,加甲醇稀释至刻度,得一系列对照品溶液,浓度分别为8.325、16.650、33.301、66.602、133.204、416.262μg/ml,分别进样10μl,峰面积分别为318001、628671、1284462、2529878、5188639、16337665,以进样浓度x(μg/ml)为横坐标、峰面积y为纵坐标绘制标准曲线,计算得回归方程为y=39315x-37471(R²=1),表明黄芩苷在8.325~416.262μg/ml范围内线性关系良好。
2.2.3供试品溶液的制备:取本品0.25g至50ml量瓶中,加入适量甲醇,60℃水浴保温15min,再超声30min,冷却后加甲醇定容至50ml,摇匀,用0.45μm微孔滤膜滤过,取续滤液即得。
2.2.4阴性溶液的制备:按肤康凝胶处方和制备工艺制备缺黄芩的阴性凝胶,按“2.2.3”项下方法制成阴性对照溶液。
2.2.5系统适应性试验:取“2.2.2”“2.2.3”“2.2.4”项下对照品溶液、供试品溶液、阴性对照溶液各适量,按“2.2.1”项下色谱条件进样测定,记录色谱图,理论塔板数按黄芩苷峰计算应不低于2500,分离度>1.5,各成分基线分离良好。供试品溶液的色谱图在与黄芩苷对照品相应保留时间处有色谱峰与之对应,而缺黄芩的阴性对照溶液在15min左右没有色谱峰,表明阴性对照对黄芩苷的测定无干扰。见图2。
2.2.6精密度试验:精密吸取“2.2.2”项下对照品溶液适量,按“2.2.1”项下色谱条件,连续进样6次,每次10μl,测定黄芩苷记录峰面积,结果,黄芩苷峰面积的RSD=0.069%(n=6),表明仪器精密度良好。
2.2.7稳定性试验:取“2.2.3”项下供试品溶液适量,分别于室温下放置0、2、4、8、12、16h时按“2.2.1”项下色谱条件进样测定,记录峰面积。结果,黄芩苷峰面积的RSD=0.341%(n=6),表明供试品溶液在室温放置16h内基本稳定。
2.2.8重复性试验:精密称取同一批样品适量,按“2.2.3”项下方法制备供试品溶液,共6份,再按“2.2.1”项下色谱条件进样测定,记录峰面积并计算含量。结果黄芩苷的RSD=2.549%,表明本方法重复性良好。
2.2.9加样回收率试验:精密称取黄芩苷对照品17.91mg,加甲醇溶解并定容至25ml,制成对照品溶液,再精密称取6份已知含量的肤康凝胶0.25g,分别精密加入对照品溶液3ml,按“2.2.3”制备。在“2.2.1”色谱条件下测定其峰面积计算加样回收率。加样回收率(%)=[(测得量-样品量)/标准量]×100%。测得平均回收率92.88%,RSD值为1.111%。说明本方法回收率较好。结果见表2。
2.2.10样品含量测定:取3批样品各适量,分别按“2.2.3”项下方法制备供试品溶液,再按“2.2.1”项下色谱条件进样测定并计算含量,结果三批样品中黄芩苷含量分别为7.504mg/g、7.661mg/g、7.528mg/g。
3讨论
肤康凝胶方中苦参为主药,具有清热燥湿、祛风杀虫的作用,治疗渗出、瘙痒、红肿皮肤病;黄芩清热燥湿、消肿止血;黄连味苦、性寒,清热燥湿、泻火解毒,两者皆为臣药,属于清热燥湿配伍的经典对药。其作为院内制剂应用于临床20余年,在皮肤病方面疗效显著。苦参碱是苦参中主要有效成分,具有广泛的生物活性,具有抗菌、抗病毒、抗炎等药理功效[5],苦参又为方中君药,与该制剂的功能主治相符,黄芩苷为黄芩的主要活性成分之一[6],也具有显著的抗菌、抗炎、抗病毒作用,由于复方制剂成分复杂,充分考虑到本方其药效物质基础为多成分共同作用,因此,本试验对苦参和黄芩进行了定量考察。
本次实验考察苦参碱含量时查阅了大量文献和参考药典供试品处理方法,比较了乙酸乙酯、二氯甲烷、三氯甲烷超声萃取的方法,萃取效果较为理想的是三氯甲烷。流动相分别考察了乙腈-无水乙醇-3%磷酸(80∶10∶10,81∶10∶9,82∶10∶8,V/V),最终确定(82∶10∶8)的流动相分离度最佳,峰形好,出峰时间合适;在测定黄芩苷的含量时,分别采用了乙腈-0.1%磷酸溶液(25∶75,24∶76,23∶77,22∶78,V/V)等不同配比流动相进行试验,由于中药成分较多且复杂,每针进样时间考察40min。结果发现,流动相配比为乙腈-0.1%磷酸溶液(25∶75,24∶76,V/V)时,黄芩苷的分离度均<1.5,当乙腈-0.1%磷酸溶液(23∶77,V/V)时分离度为2.2,峰形较好,分离度、峰面积均合适,保留时间约15min,在35min中左右时,样品仍有出峰。而乙腈-0.1%磷酸溶液(22∶78,V/V)分离度高达21,保留时间约21min,相应进样时间40mim后,还有样品峰出现,进样时间大大增加。最终选择流动相为乙腈-0.1%磷酸溶液(23∶77,V/V)。
综上所述,本试验中苦参碱和黄芩苷的含量测定,方法特征性强,无阴性干扰,分离度、重复性、稳定性、加样回收率均符合要求,且所测3批样品含量稳定,说明该方法可行,可作为该制剂的含量测定方法。结果表明所建立的定量方法能较好地控制肤康凝胶质量,提高了药品质量的可控性。——论文作者:甘灿云陈海红杨海燕
声明:①文献来自知网、维普、万方等检索数据库,说明本文献已经发表见刊,恭喜作者.②如果您是作者且不想本平台展示文献信息,可联系学术顾问予以删除.

SCISSCIAHCI